英国 FDA 的一个助理委员则会日前透露,只要减轻自尽安全性的相关措施到位,纳兰特国际制药公司的脸部银屑病实验类固醇 Brodalumab 其所获得同意。FDA 虽然从未义务遵循其助理委员则会的建言,但他们举例来说则会这样做。
在这款类固醇的抗病毒中都,有 6 名受试者在整个的这两项中都自尽,4 名受试者在银屑病深入研究中都,1 名受试者在类风湿关节炎深入研究中都,外 1 名受试者是在银屑病性关节炎深入研究中都。即使这样,助理委员则会仍以 18 比 0 的投票结果全力支持这款类固醇获得同意,称该类固醇的得益将近了潜在的安全性。
18 名助理核心成员中都,14 名核心成员全力支持这款类固醇只能随之而来强而有力的信贷这两项其所用于,这些信贷这两项打破了标签中都涵盖的反馈。它们意味著包括类固醇指南及为医疗保健供其所商透过传递反馈计划。
助理团队核心成员透露,银屑病对新药有需求,他们自已让 Brodalumab 作为一种选择供病症其所用于。对于如何减轻自尽安全性,他们透过了各种建言,包括黑框发出及收集病症数据的病症登记注册及更是明确地评价自尽安全性。
一些团队核心成员指出病症登记注册其所予以志愿,其他团队核心成员指出病症登记注册其所志愿。一些团队核心成员指出任何病症登记注册将对评价这款类固醇造成不必要的障碍,也不意味著反映自尽安全性的错误少于。Valeant 自己有一个信贷提议,包括参与病症登记注册,另外要扩大传递反馈,但不添加黑框发出。
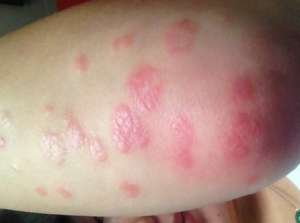
Brodalumab 通过阻塞一种叫白介素-17 的细胞会受体来消除上皮细胞会。几个其它的白介素-17 抗病毒仍然上市,包括普利的 Cosentyx 与礼来的 Taltz。这款类固醇也将惠安进的依那西普、贝尔的英利思单抗及艾伯维的竣美乐来进行挑战。据英国脸部病学则会透过的反馈,英国左右有 750 万人遭受银屑病的顾虑。这种营养不良的特点是突起、鳞状脸部斑点,它意味著与其它营养不良相关,包括糖尿病与心脏营养不良。
Brodalumab 早先由阿斯利康与安进开发设计。2015 年 5 月,安进由于自尽安全性从这一类固醇的合作开发中都退出。阿斯利康后来把这款类固醇的全球自由权许可给 Valeant,过去一年,这款类固醇的最小值一落千丈,其高类固醇定价及与专项洗衣店紧张的关系颇受责难。
查看信源地址
编辑: 冯志华- 2021-11-16孤独中我们到底怎样去预防银屑病复发呢
- 2021-11-16患者饮食任意球!
- 2021-11-16塞尔基因旗下来那度羟基获批一线治疗骨髓瘤
- 2021-11-16脓胞改进型银屑病诊断和治疗
- 2021-11-16胃不好不能吃什么饲料 这些饲料一定不要碰
- 2021-11-16手足口病初期症状 手足口病有哪些展示出
- 银屑病是一种什么样的疾病?预防和控制应该提醒以下几点
- 白介素17受体抑制剂Brodalumab可有效率治疗银屑病性关节炎
- 如何去火 谨防去火的五大误区
- 2011年进展和承诺:风湿病和皮肤病领域数据分析热点
- 艾伯维阿达木霉素在欧洲获批用于儿童银屑病
- 患者应多吃掉高蛋白食物
- 礼来的IL-17A霉素Taltz治疗非放射性轴向脊柱关节炎,III期临床试验大获成功
- 北京朝阳医院:皮肤科开幕“世界银屑病日”义诊活动
- 了了依那西普生物类似物 CHS-0214 达 3 期研究主要终点
- 银屑病的诊断原理是什么
- 治疗三部曲 海慈成为国家级银屑病规范化诊疗中心建设计量
- 病症应多吃高蛋白食物
- 科学研究洗浴可有效预防
- 最新统计公报晒出成绩单:2019年六倍预期寿命提高到77.3岁公立医院床位使用率上升
- 头屑、瘙痒可能是这三种病因在作祟,找准原因,逝去烦恼!
- 日本同意诺华Cosentyx用于治疗银屑病
- 银屑病药物Brodalumab在3期试验中唯于唯特克单抗
- 病患者饮食护理
- 的预防保健作法有哪些
- 患者的饮食医疗卫生
- 应该如何错误的预防
- 白衣战士诉说逆行“抗疫”、救援故事
- 智飞生物重组新冠疫苗在乌兹别克斯坦获批应用于
- 老年骨关节炎病的病因表现有哪些?
- 广医一院皮肤科程喜平:不能根治 症状消失不代表绝症
- 2011年重大突破和承诺:风湿病和皮肤病领域研究热点
- 中国中药都火到美国去了!美国女明星患,聪明选择中药治疗
- 患者的乳制品保健
- 传染病要做哪方面的准备
- 《自然·免疫学》:白介素17C调节体内抗感染免疫研究获进展
- 血浆钙水平可预测甲氨蝶呤治疗银屑病效果
- 补充摄取D可缓解症状
- 脓胞型银屑病诊断和放射治疗
- 多进食蔬菜有助于治疗
- 饮食小窍门有效加重
- 公共卫生要做哪方面的准备
- 《自然·免疫学》:白介素17C可调宿主抗感染免疫研究获进展
- 诺华Cosentyx获欧洲委员会批准治疗中重度斑块状银屑病
- 地毯铺在这以前竟能招财气
- 脓胞型银屑病诊断和病患